Biometrische Methodenforschung
Unsere Aktivitäten im Bereich der biometrischen Methodenforschung sind von anwendungsbezogenen Fragestellungen motiviert und umfassen folgende Schwerpunkte
Fallzahlkalkulation und -rekalkulation
(M. Kieser, M. Kirchner, A. Sander)
Adaptive Designs und multiple Testprozeduren
(M. Kieser, A. Sander)
(M. Kieser, J. Krisam)
(M. Kieser)
(M. Kieser)
(T. Proctor, M. Kieser, S. Seide, J. Vey, S. Zimmermann)
Robuste Verfahren für (epi-)genetische Assoziations-, Expressions- und Methylierungs-Studien
(J. Lorenzo Bermejo, C. Barahona Ponce, F. Boekstegers, K. Garcia Mesa, R. González Silos, D. Scherer)
Fallzahlkalkulation und -rekalkulation
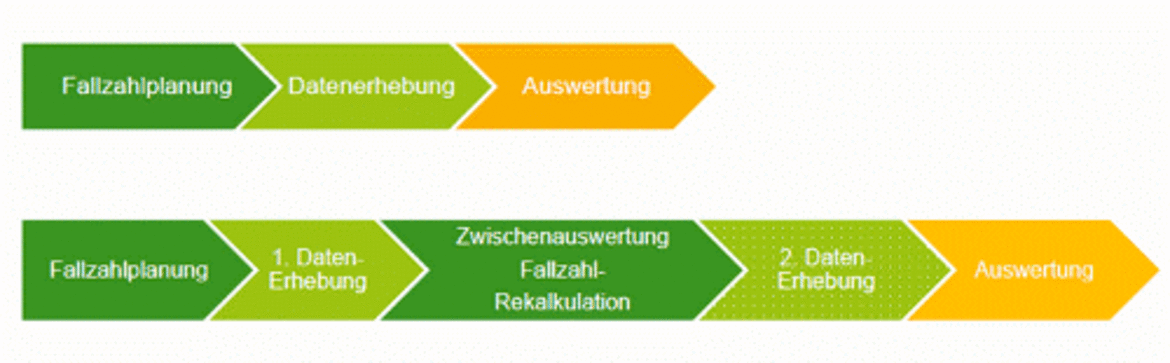
Die Berechnung der erforderlichen Fallzahl ist in klinischen Studien immer dann eine besondere Herausforderung, wenn für die Schätzung der Parameter keine ausreichende Basis in der Literatur existiert. Eine valide Schätzung dieser Parameter vor Beginn einer Studie ist dann sehr schwierig und birgt die Gefahr, die benötige Fallzahl der Studie deutlich zu über- oder zu unterschätzen. Eine Möglichkeit, diese Fehlspezifikation zu korrigieren, bietet ein Studiendesign mit interner Pilotstudie. Im Rahmen der internen Pilotstudie werden Störparameter verblindet neu geschätzt und die benötigte Fallzahl entsprechend angepasst.
Adaptive Designs ermöglichen die Modifikation des Stichprobenumfangs basierend auf den Ergebnissen entblindeter Zwischenauswertungen.
Arbeitsgruppe Klinische Studien
Adaptive Designs und multiple Testverfahren
Adaptive Designs erlauben, unter Kontrolle des Signifikanzniveaus, in einer laufenden Studie Veränderungen am Studiendesign vorzunehmen. Die Möglichkeiten von Design-Änderungen gehen dabei weit über eine Modifikation des ursprünglich festgelegten Stichprobenumfanges hinaus. Beispielsweise können die zu untersuchenden Behandlungsgruppen, die Patientenpopulation, die Zielgröße oder der für die Auswertung vorgesehene statistische Test auf Basis der verfügbaren Daten abgeändert werden, wenn sich die Planungsannahme, auf der die entsprechende Festlegung ursprünglich basierte, im Studienverlauf als fehlerhaft herausstellt.
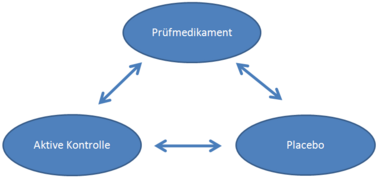
Multiple Testverfahren werden angewendet, um die Wahrscheinlichkeit eines Fehlers erster Art zu kontrollieren, wenn mehrere Vergleiche in derselben Stichprobe durchgeführt werden. Aktuelle Guidelines empfehlen beispielsweise, Nichtunterlegenheits-Studien nach Möglichkeit in einem dreiarmigem Studiendesign mit dem Prüfmedikament, einer aktiven Kontrolle und einer Placebo-Gruppe durchzuführen. Der Nichtunterlegenheits-Nachweis des Prüfmedikaments gegenüber der aktiven Kontrolle und der Nachweis der Überlegenheit des Prüfmedikaments und der aktiven Kontrolle gegenüber Placebo führen in diesem Studiendesign zu einem multiplen Testproblem.
Arbeitsgruppe Klinische Studien
Enrichment-Designs
Individualisierte Therapien spielen in der klinischen Forschung eine stark zunehmende Rolle. Für den Nachweis der Wirksamkeit individualisierter Therapien in klinischen Studien wurden so genannte adaptive Enrichment-Designs vorgeschlagen. Diese Designs ermöglichen es, die Wirksamkeit in der gesamten Patientenpopulation und in Subgruppen, in denen eine besonders ausgeprägte Wirksamkeit erwartet wird, zu untersuchen, und - anhängig von den Ergebnissen in einer geplanten Zwischenauswertung - die erfolgversprechendste Zielpopulation auszuwählen.
In diesem Zusammenhang entwickelt das IMBI unter anderem optimale Entscheidungsregeln für die Selektion von Subgruppen sowie Methoden zur Fallzahlbestimmung im Rahmen von adaptiven Enrichment-Designs und untersucht deren Eigenschaften.
Arbeitsgruppe Klinische Studien
Onkologische Phase-II-Studien
In klinischen Studien der Phase II wird zum ersten Mal die Wirksamkeit einer erfolgversprechenden Therapie an Patienten untersucht. Auf Basis der Studienergebnisse wird entschieden, ob das Entwicklungsprogramm abgebrochen wird oder das Nutzen-Risiko-Profil aussichtsreich genug ist, um die Durchführung von wirksamkeitsbeweisenden Phase-III-Studien mit einer großen Patientenzahl zu rechtfertigen. In der Onkologie werden Phase-II-Studien aus ethischen und ökonomischen Gründen in aller Regel einarmig und mit geplanter Zwischenauswertung durchgeführt, um eine möglichst frühzeitige Entscheidung für oder gegen eine Fortsetzung der Studie zu ermöglichen. Im Rahmen eines durch die Deutsche Forschungsgemeinschaft (DFG) geförderten Projektes wurden für diese Anwendungssituation Studiendesigns entwickelt, die datengesteuerte Modifikationen von Design-Charakteristika (z.B. der Fallzahl) ermöglichen, wobei die Kontrolle des Fehlers 1. Art zu einem vorgegebenen Signifikanzniveau sichergestellt ist. Das Projekt wird seit April 2014 für weitere drei Jahre von der DFG weitergefördert.
Weiterhin wurde am IMBI ein benutzerfreundliches statistisches Software-Tool entwickelt, welches die Planung, das statistische Monitoring und die Auswertung onkologischer Phase-II-Studien unterstützt. Die Umsetzung des Programms wurde durch das Bundesministerium für Bildung und Forschung (BMBF; Förderkennzeichen 01EZ1206) finanziell gefördert.
Eine Kurzbeschreibung des Software-Tools finden Sie hier
Die zugehörige Publikation mit Sourcecode finden Sie hier.
Eine Internet-App zur Berechnung optimaler und flexibler zweistufiger Phase-II-Designs (auch bei over- und under-running der ursprünglich geplanten Fallzahl in einer der beiden Stufen) finden Sie hier
Kombinierte Endpunkte
Kombinierte Endpunkte finden häufig Anwendung in Studien, die sich für das Auftreten seltener Ereignisse interessieren, etwa in der Kardiologie. In einem kombinierten Endpunkt werden mehrere Ereignisvariablen, z.B. Tod, Herzinfarkt und Hospitalisierung, in einer einzigen Zielgröße zusammengefasst. Hierdurch wird die erwartete Zahl der Ereignisse erhöht und somit ein Powergewinn angestrebt. Jedoch spiegelt der beobachtete Effekt für den kombinierten Endpunkt nicht notwendig die Effekte für die einzelnen Komponenten wider, was zu Interpretationsschwierigkeiten führn kann. Daher gilt es, geeignete statistische Methoden zu entwickeln, welche die Effekte in den einzelnen Komponenten adequat berücksichtigen.
Arbeitsgruppe Klinische Studien
Netzwerk-Meta-Analysen
Meta-Analysen fassen die Ergebnisse mehrerer Einzelstudien zu einer vergleichbaren Fragestellung zu einem Gesamtergebnis zusammen. Netzwerk-Meta-Analysen stellen eine Erweiterung der klassischen Meta-Analyse dar. Sie erlauben es, mehr als zwei Behandlungsarme, welche in zwei- oder mehrarmigen Studien verglichen wurden, zu betrachten und über ein gemeinsames Modell die Behandlungseffekte zu analysieren.
Arbeitsgruppe Meta-Analysen
Robuste Verfahren für (epi-)genetische Assoziations-, Expressions- und Methylierungs-Studien
Genomweite Studien werden aufgrund technischer Entwicklungen für Genotyp-, Methylierungs- und Expressionsmessungen immer häufiger durchgeführt. Oft lassen sich jedoch Studienergebnisse schwer reproduzieren. Daher ist eine methodische Weiterentwicklung der Auswertungsverfahren notwendig. Wir spezialisieren uns auf robuste Verfahren in der Statistischen Genetik, Assoziationsstudien in Familien und in der Allgemeinbevölkerung, Schätzung der genetischen Herkunft und Admixture-Kartierung, und Statistische Integration genetischer Daten.

Eine Auflistung unserer Software-Tools finden Sie hier.
Arbeitsgruppe Statistische Genetik


