Forschungsgruppe Kopf-Hals-Tumore
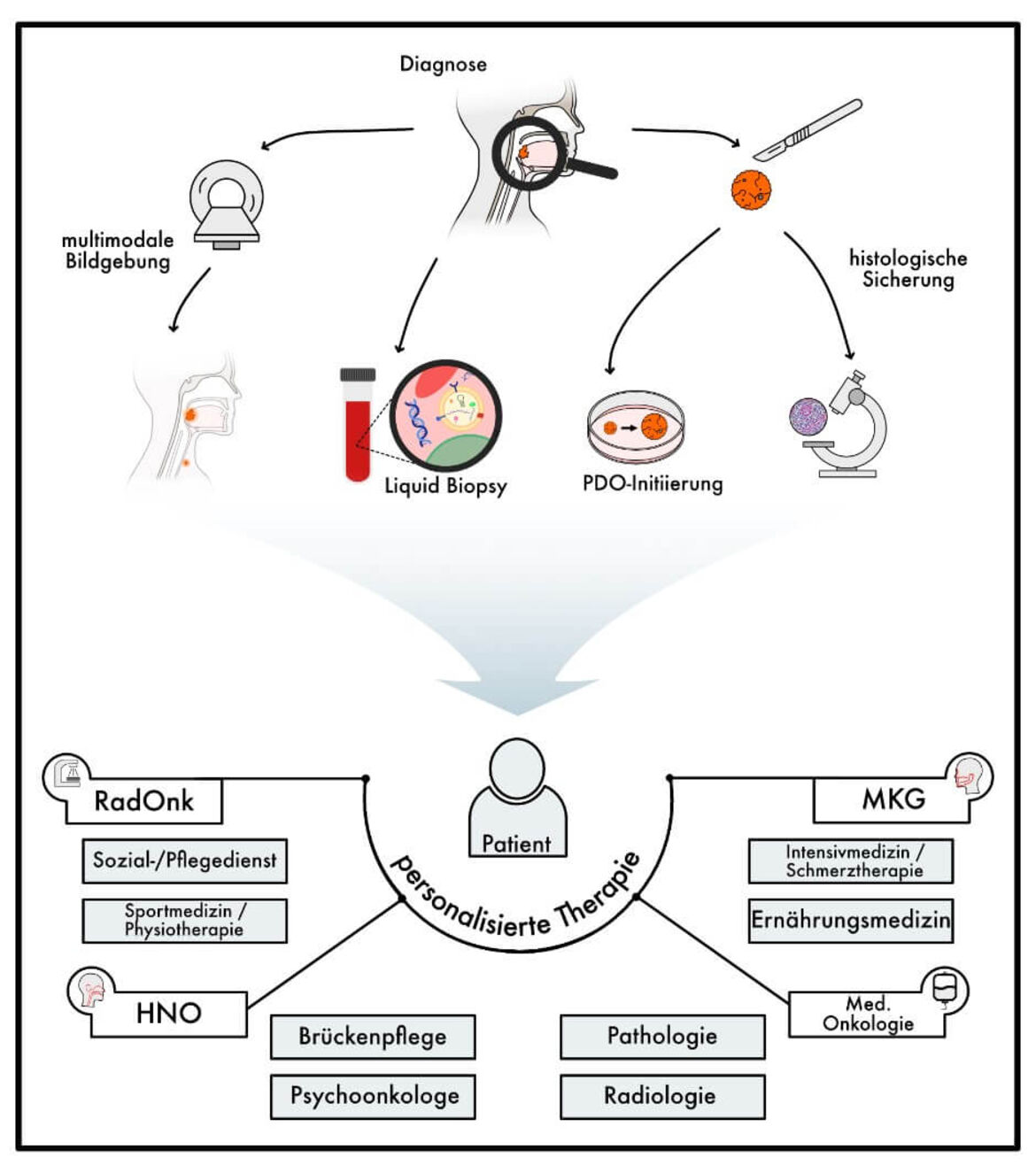
Kopf-Hals-Tumore bilden eine heterogene Gruppe von Tumorerkrankungen in dieser Region. Die häufigsten bösartigen Tumore dieser Region sind Plattenepithel-Karzinome, seltener kommen Karzinome des Nasopharynx, der Nasenhaupt- und Nasennebenhöhlen, mucosale Melanome sowie Speicheldrüsentumore vor. Zentraler Ansatzpunkt für die Behandlung von Kopf-Hals-Tumoren ist eine enge interdisziplinäre Abstimmung und Kooperation aller beteiligter Fachabteilungen: Strahlentherapie, medizinische Onkologie (NCT), Hals-Nasen-Ohren-Heilkunde (HNO) und Mund-Kiefer-Gesichtschirurgie (MKG).
Unser Ziel ist es, präzise und personalisierte Behandlungsoptionen für Patienten mit Kopf-Hals-Tumoren zu entwickeln. Dabei legen wir Wert auf gegenseitige Unterstützung und eine wertschätzende Atmosphäre. Wir haben viel Freude daran, mit verschiedenen Fachdisziplinen und Kooperationspartnern zusammenzuarbeiten. Gemeinsam integrieren wir im Rahmen translationaler Forschungsprojekte, innovative Strategien zeitnah in die klinische Praxis, um sowohl die Heilungschancen als auch die Lebensqualität unserer Patienten nachhaltig zu verbessern.
Ausschreibungen
Doktoranden
Interessieren Sie sich für unsere Arbeit und möchten sich aktiv an unserer Forschung beteiligen? Es besteht die Möglichkeit als wissenschaftliche Hilfskraft und/oder Doktorand in unserer Arbeitsgruppe mitzuarbeiten. Wir führen keine aktualisierte Themenliste, besprechen aber sehr gerne gemeinsam mögliche Projekte. Für Fragen oder Bewerbungen schreiben Sie bitte eine E-Mail an: E-Mail
Bitte fügen Sie Ihrer Bewerbung folgende Unterlagen bei:
- kurzes Motivationsschreiben
- CV
Fellowship
The Head and Neck Radiation Oncology Fellowship at Heidelberg University Hospital offers specialized, in-depth training for physicians dedicated to the treatment of head and neck cancer. This one-year program provides extensive clinical experience in the management of head and neck tumors, while also offering opportunities to participate in cutting-edge translational research aimed at advancing the field.
The Head and Neck Tumor Center in Heidelberg, certified as an Organ Cancer Center since 2019, treats over 300 newly diagnosed patients with head and neck malignancies annually. Fellows will also have the opportunity to gain experience with particle therapy at the Heidelberg Ion Beam Therapy Center (HIT) and will play an active role in patient care, collaborating closely with multidisciplinary teams to develop and implement treatment plans.
A key focus of the fellowship is the integration of clinical practice with the latest advancements in research. This includes the application of biomarkers and molecular profiling to refine and personalize treatment strategies. Fellows will gain exposure to a wide variety of cases, including rare and complex head and neck tumors, ensuring a comprehensive learning experience.
This fellowship represents an exceptional opportunity for radiation oncologists seeking to advance their expertise in the treatment of head and neck cancers and develop specialized clinical and research skills in this area.
1. Requirements
- Specialization in radiation oncology: Candidates should be nearing the completion of their specialist training or already certified as specialists in radiation oncology.
- Participation in clinical and translational research: Candidates are expected to actively engage in clinical and translational research projects.
2. How to Apply
Interested applicants are encouraged to contact PD Dr. Thomas Held (E-Mail) to begin the application process.
3. Stipends
The fellowship provides compensation for a clinician scientist position based on the reference salary of Heidelberg University Hospital.
Arbeitsgruppe

ÄRZTLICHE MITARBEITER-/INNEN
Kooperationspartner
Prof. Dr. Dr. Amir Abdollahi
Prof. Dr. Peter Huber
Klinische Kooperationseinheit Molekulare Radioonkologie – Deutsches Krebsforschungszentrum (DKFZ)
Prof. Dr. Klaus Maier-Hein
Abteilung Medizinische Bildverarbeitung – Deutsches Krebsforschungszentrum (DKFZ)
Prof. Dr. Lena Maier-Hein
Abteilung Intelligente Medizinische Systeme – Deutsches Krebsforschungszentrum (DKFZ)
Dr. Jens Puschhof
Nachwuchsgruppe Epithel-Mikrobiom-Interaktionen (EMIL) – Deutsches Krebsforschungszentrum (DKFZ)
Dr. Sebastian Regnery
Prof. Dr. Holger Sültmann
Abteilung Krebsgenomforschung – Deutsches Krebsforschungszentrum (DKFZ)
MIRO-Team
Forschungsschwerpunkte
Liquid Biopsy
Die Liquid Biopsy ist ein modernes, nicht-invasives Verfahren, das in der Krebstherapie zunehmend an Bedeutung gewinnt. Sie ermöglicht die Analyse von Biomarkern im Blut, wie zirkulierender Tumor-DNA (ctDNA), und unterstützt die kontinuierliche Überwachung des Tumors. Dadurch kann die Therapie individuell angepasst und verbliebene Tumorzellen oder Rezidive frühzeitig erkannt werden.
Im Rahmen folgender klinischer Studien kommen Liquid Biopsies zum Einsatz:
- CARE – Sicherheit und Toxizität der Re-Radiotherapie mit Kohlenstoffionen bei Kopf-Hals-Tumoren Link zur CARE-Studienseite
- MIGNITE – Verbesserung der Immunprotektion durch Volumendeeskalation in der definitiven Radio(chemo)therapie Link zur MIGNITE-Studienseite
- CORPORAL – Personalisierung der Tumortherapie mit Organoidmodellen Link zur CORPORAL-Studienseite
- NAVIGATORR – Verbesserung der lokalen Tumorkontrolle durch präzise Resektion und interdisziplinäre Kooperation Link zur NAVIGATORR-Studienseite
- PROFOUND-HN – Volumendeeskalation in der postoperativen Radiotherapie Link zur PROFOUND-Studienseite
Patient-derived Organoids
Tumor-Organoide (engl.: patient-derived organoids, PDOs) sind dreidimensionale Modelle, die aus Tumorgewebe von Patienten, welches im Rahmen von Biopsien oder Operationen gewonnen wird, angezüchtet werden. Sie bewahren die genetischen und molekularen Eigenschaften des ursprünglichen Tumors, was sie zu idealen Modellen in der Entwicklung und Optimierung einer personalisierten Therapie macht.
Folgende klinische Studien beinhalten PDOs:
- CORPORAL – Personalisierung der Tumortherapie mit Organoidmodellen Link zur CORPORAL-Studienseite
- NAVIGATORR – Verbesserung der lokalen Tumorkontrolle durch präzise Resektion und interdisziplinäre Kooperation Link zur NAVIGATORR-Studienseite
- PROFOUND-HN – Volumendeeskalation in der postoperativen Radiotherapie Link zur PROFOUND-Studienseite
Volumendeeskalation
In der Behandlung von Patienten mit Kopf-Hals-Tumoren ist wichtig, das elektive Zielvolumen differenziert festzulegen. Einerseits sollen jene Bereiche behandelt werden, in denen ein relevantes Risiko für okkulte Metastasen besteht, anderseits gesunde Strukturen geschont und Nebenwirkungen minimiert werden. Molekulare Bildgebung ermöglicht eine sensitivere Beurteilung der Tumorausbreitung und bietet damit Potential, das elektive Bestrahlungsvolumens bei effektiver Tumorkontrolle zu verkleinern und die Verträglichkeit der Bestrahlung zu verbessern.
Folgende Studien prüfen eine Volumendeeskalation in der Radiotherapie von Patienten mit Kopf-Hals-Tumoren:
- MIGNITE – Verbesserung der Immunprotektion durch Volumendeeskalation in der definitiven Radio(chemo)therapie Link zur MIGNITE-Studienseite
- PROFOUND-HN – Volumendeeskalation in der postoperativen Radiotherapie Link zur PROFOUND-Studienseite
Immunprotektion
Ein reaktionsfähiges körpereigenes Immunsystem ist für die erfolgreiche Bekämpfung von Tumorerkrankungen wichtig und unterstützt die medizinische Tumortherapie. Da durch die Bestrahlung nicht nur der Tumor, sondern auch das Immunsystem geschwächt wird, ist es Gegenstand aktueller Forschung, diesen unerwünschten Effekt – zum Beispiel durch eine Reduktion des Bestrahlungsvolumens – zu minimieren und die Effektivität der Therapie zu steigern.
Folgende klinische Studien untersuchen die Immunprotektion im Rahmen der Radiotherapie:
- MIGNITE – Verbesserung der Immunprotektion durch Volumendeeskalation in der definitiven Radio(chemo)therapie Link zur MIGNITE-Studienseite
- INTERACT – Evaluation der SBRT bei metastasierten Erkrankungen Link zur INTERACT-Studienseite
Partikeltherapie und Boost-Konzepte
Partikeltherapie und Boost-Konzepte ausgeklappt
Ionenstrahlung erlaubt eine präzisere Fokussierung der Dosis auf den Tumor und schont das umliegende Gewebe maximal. Die Bestrahlung mit Schwerionen, wie z.B. Kohlenstoffionen, ist bei bestimmten Tumorarten biologisch wirksamer. Die Partikeltherapie hat sich bei manchen Tumoren, wie Speicheldrüsentumoren und Schädelbasistumoren, als überlegen erwiesen. Sie kann als alleinige Therapie oder zur Dosisaufsättigung im Rahmen von Boost-Konzepten angewandt werden.
Aktuelle klinische Studien, die eine Partikeltherapie beinhalten:
- ACCO – Lokoregionäre Strahlentherapie mit Kohlenstoffionen (C12) versus Photonen-IMRT mit Kohlenstoffionen-Boost Link zur ACCO-Studienseite
- CARE – Sicherheit und Toxizität der Re-Radiotherapie mit Kohlenstoffionen bei Kopf-Hals-Tumoren Link zur CARE-Studienseite
- MIGNITE – Verbesserung der Immunprotektion durch Volumendeeskalation in der definitiven Radio(chemo)therapie Link zur MIGNITE-Studienseite
Stereotaktische Radiotherapie
Die stereotaktische Body-Radiotherapie (SBRT) ermöglicht eine präzise Behandlung mit wenigen Bestrahlungstagen und ist fester Bestandteil der Behandlung metastasierter Krebserkrankungen. Sie führt zu einer effektiven lokalen Kontrolle und einem längeren progressionsfreien Überleben. Strahlennebenwirkungen sind selten, und aktuelle Forschung untersucht Wege, die Anwendung der SBRT weiter zu verbessern.
Aktuelle klinische Studien zur SBRT:
- INTERACT – Integration der SBRT in systemische Behandlungsansätze für Patienten mit metastasierter Tumorerkrankung Link zur INTERACT-Studienseite
Re-Radiotherapie
Nach einer initialen Therapie von Kopf-Hals-Tumoren erleiden 30-50% der Patienten ein lokales Rezidiv, für das die Behandlungsoptionen begrenzt sind. Eine Re-Radiotherapie kann eine wertvolle Möglichkeit zur lokalen Kontrolle bieten, wobei besondere Rücksicht auf die Vorbelastung des Gewebes genommen werden muss. In diesem Zusammenhang zeigt die Kohlenstoffionen-Bestrahlung vielversprechende Ergebnisse.
Laufende klinische Studie zur Re-Radiotherapie:
- CARE – Sicherheit und Toxizität der Re-Radiotherapie mit Kohlenstoffionen bei Kopf-Hals-Tumoren Link zur CARE-Studienseite
Multimodale Bildgebung
Durch den Einsatz verschiedener Bildgebungsmodalitäten können genauere Informationen über die Tumorlokalisation und eventuell vorhandene Metastasen erlangt werden. Dies ermöglicht eine angepasste Zielvolumendefinition, was letztlich zu einer verbesserten Präzision führt und damit eine Steigerung der Wirksamkeit und Minimierung von Nebenwirkungen zur Folge hat.
Folgende klinische Studien beschäftigen sich mit dem Einsatz diverser Bildgebungsmodalitäten in der Radiotherapie:
- OLYMPIC – MSOT als diagnostische Maßnahme zur Hypoxie-Darstellung Link zur OLYMPIC-Studienseite
- PROFOUND-HN – Volumendeeskalation in der postoperativen Radiotherapie Link zur PROFOUND-Studienseite
- MIGNITE – Verbesserung der Immunprotektion durch Volumendeeskalation in der definitiven Radio(chemo)therapie Link zur MIGNITE-Studienseite
Automatisierung
Die Automatisierung in der Strahlentherapie ermöglicht eine schnelle und standardisierte Therapieplanung. Durch den Einsatz künstlicher Intelligenz können Zielvolumina Guideline-basiert erstellt werden und anschließend vom behandelnden Arzt angepasst werden. Dies steigert die Effizienz und Konsistenz in der Zielvolumendefinition. Automatisiert erstellte Bestrahlungspläne bieten Potential für eine effiziente und präzise Therapieplanung und -optimierung im Verlauf der Behandlung.
Studien
ACCO
Ist Radiotherapie mit Kohlenstoffionen der bimodalen Radiotherapie in Bezug auf die lokale Kontrolle beim adenoid-zystischen Karzinom überlegen?
Zusammenfassung
Die ACCO-Studie untersucht adenoidzystische Karzinome (ACC) der Kopf-Hals-Region, die nach Operationen oft rezidivieren und strahlenresistent sind. Bisher wurde eine Kombination aus Kohlenstoffionen- und Photonenbestrahlung (bimodale Radiotherapie) angewendet, die der alleinigen Photonenbestrahlung überlegen ist. Die Studie prüft, ob eine alleinige Kohlenstoffionenbestrahlung die Tumorkontrolle weiter verbessern kann.
In der randomisierten Phase-II-Studie werden zwei Therapien verglichen: eine alleinige Kohlenstoffionenbestrahlung (4 Wochen, 22 Fraktionen) und die Standardtherapie mit Kohlenstoffionen und Photonen (6,5 Wochen, 33 Fraktionen). Ziel ist es, die lokoregionäre Kontrolle, das progressionsfreie Überleben, die Toxizität und die Lebensqualität zu bewerten. 314 Patienten sollen über fünf Jahre nachbeobachtet werden. Die Studie wird von der Deutschen Krebshilfe gefördert und rekrutiert seit Dezember 2019.
Wichtigste Einschlusskriterien
- Histologisch gesichertes adenoidzystisches Karzinom im Kopf-Hals Bereich
- Indikation zur Bestrahlung: nicht-operabel oder R1/R2 reseziert oder Perineuralscheiden Invasion (Pn+) oder pT3/pT4
- Alter 18-80 Jahre
Wichtigste Ausschlusskriterien
- Stadium IV (Fernmetastasen, außer: pulmonale Rundherde < 1 cm)
- Lymphknotenbefall (klinisch oder pathologisch)
Publikationen
Lang, K., Adeberg, S., Harrabi, S., Held, T., Kieser, M., Debus, J., & Herfarth, K. (2021). Adenoid cystic Carcinoma and Carbon ion Only irradiation (ACCO): Study protocol for a prospective, open, randomized, two-armed, phase II study. BMC cancer, 21(1), 812. https://doi.org/10.1186/s12885-021-08473-5
CARE
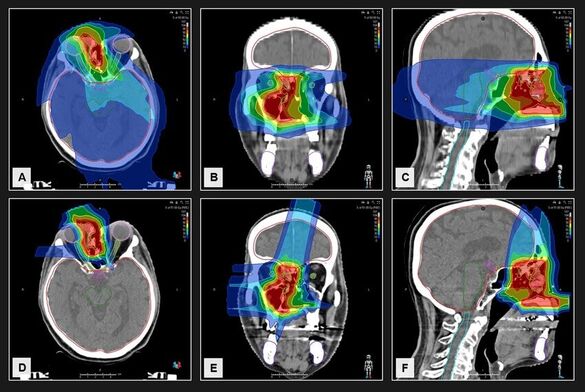
Wie ist die Wirksamkeit und Verträglichkeit der Re-Radiotherapie mit Kohlenstoffionen im Vergleich zu Photonen bei Patienten mit rezidivierten Kopf-Hals-Tumoren?
Zusammenfassung
Die Studie untersucht Kohlenstoff Ion Re-Radiotherapie bei Patienten mit rezidivierenden Kopf-Hals-Tumoren im Vergleich zu einer Intensitätsmodulierten-Radiotherapie (IMRT). Die Studie beinhaltet ein breites translationales Programm mit Bestimmung der zirkulierenden Tumor-DNA im longitudinalen Verlauf, als auch die prospektive Auswertung bildgebender MRT Parameter.
Wichtigste Einschlusskriterien
- Lokal rezidivierte / progrediente Kopf-Hals-Tumorerkrankung nach initialer Radiotherapie
- Mikroskopischer oder makroskopischer Tumorrest nach Salvage-Operation
- Indikation zur Re-Radiotherapie
- Karnofsky-Performance-Score ≥ 60
- Alter ≥ 18 Jahre
Wichtigste Ausschlusskriterien
- Re-Bestrahlung eines Larynxkarzinoms
- Diagnostiziertes Plasmozytom, Sarkom oder Chordom
- Zeitintervall < 6 Monate nach der initialen Strahlentherapie
- Fernmetastasen (außer Lungenmetastasen)
- Patienten, die sich nicht von akuten Toxizitäten vorheriger Therapien erholt haben
Publikationen
Janke, F., Stritzke, F., Dvornikovich, K., Franke, H., Angeles, A. K., Riediger, A. L., Ogrodnik, S., Gerhardt, S., Regnery, S., Schröter, P., Bauer, L., Weusthof, K., Görtz, M., Harrabi, S., Herfarth, K., Neelsen, C., Paech, D., Schlemmer, H. P., Abdollahi, A., Adeberg, S., Debus J., Sültmann H., Held, Th. (2024). Early circulating tumor DNA changes predict outcomes in head and neck cancer patients under re-radiotherapy. International journal of cancer, 10.1002/ijc.35152. Advance online publication. https://doi.org/10.1002/ijc.35152
Held, Th., Tessonnier, T., Franke, H., Regnery, S., Bauer, L., Weusthof, K., Harrabi, S., Herfarth, K., Mairani, A., Debus, J., & Adeberg, S. (2022). Ways to unravel the clinical potential of carbon ions for head and neck cancer reirradiation: dosimetric comparison and local failure pattern analysis as part of the prospective randomized CARE trial. Radiation oncology (London, England), 17(1), 121. https://doi.org/10.1186/s13014-022-02093-4
Held, Th., Lang, K., Regnery, S., Weusthof, K., Hommertgen, A., Jäkel, C., Tonndorf-Martini, E., Krisam, J., Plinkert, P., Zaoui, K., Freudlsperger, C., Moratin, J., Krauss, J., Harrabi, S. B., Herfarth, K., Debus, J., & Adeberg, S. (2020). Carbon ion reirradiation compared to intensity-modulated re-radiotherapy for recurrent head and neck cancer (CARE): a randomized controlled trial. Radiation oncology (London, England), 15(1), 190. https://doi.org/10.1186/s13014-020-01625-0
CORPORAL
Ist Radiotherapie mit Kohlenstoffionen der bimodalen Radiotherapie in Bezug auf die lokale Kontrolle beim adenoid-zystischen Karzinom überlegen?
Zusammenfassung
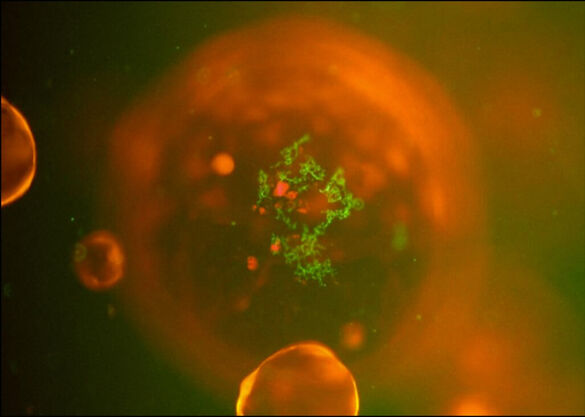
Im Rahmen dieser Studie werden aus frischem Tumorgewebe, welches in Biopsien oder Operationen gewonnen wird, Tumor-Organoide (engl.: patient-derived tumor organoids, PDOs) angezüchtet. Die Organoide stellen kleine Kopien der Original-Gewebe im Patienten dar und bilden diese strukturell und genetisch nach. Die Organoide werden genomisch, transkriptomisch, proteomisch, mikrobiomisch und metabolomisch analysiert mit einem Fokus auf das Ansprechen von Tumor-Organoiden auf verschiedene Bestrahlungsdosen mit und ohne Medikamente.
Das übergreifende Ziel der Studie ist es, eine biologisch personalisierte Radiotherapie zu ermöglichen. PDOs sollen zur Prädiktion des Ansprechens einer Bestrahlung im Patienten genutzt werden und somit die biologisch personalisierte Dosisverschreibung und Wahl simultaner Therapie zu ermöglichen. Zusätzlich zu den PDOs werden auch Tumor-Derivate aus dem peripheren Blut (engl.: liquid biopsy) sowie Speichelproben zum Monitoring des oralen Mikrobioms der Patienten gewonnen. Darauf basierend wird die Interaktion zwischen Tumor, Mikrobiom und Immunzellen charakterisiert.
Wichtigste Einschlusskriterien
⦁ Patienten mit soliden Tumoren, die am Universitätsklinikum Heidelberg eine Tumorresektion oder Biopsie erhalten
⦁ Patienten mit Nicht-Tumor-Erkrankungen, die eine Geweberesektion oder diagnostische Biopsie am Universitätsklinikum Heidelberg erhalten
⦁ Alter ≥ 18 Jahre
Wichtigste Ausschlusskriterien
Ablehnung der Studienteilnahme durch den Patienten
INTERACT
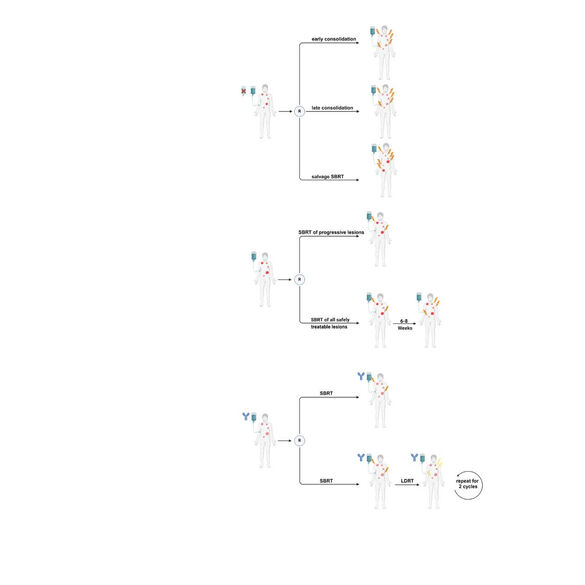
Wann sollte die SBRT bei Patienten mit metastasierten Erkrankungen als konsolidierende bzw. Salvage-Therapiemaßnahme eingesetzt werden?
Zusammenfassung
INTERACT zielt darauf ab, die Integration der stereotaktischen Körperstrahlentherapie (SBRT) in systemische Krebsbehandlungen für Patienten mit metastasierter Erkrankung zu optimieren. INTERACT umfasst ein Register in Form einer multizentrischen Beobachtungs- und Biomarkerstudie und eine randomisierte, interventionelle, mehrarmig Phase-II-Studie.
Aktuelle Studien haben gezeigt, dass SBRT generell sicher ist und in Kombination mit Systemtherapie hochwirksam in der Behandlung metastasierender Krebserkrankungen sein kann. Dennoch bleiben grundlegende Fragen zum Zeitpunkt der SBRT, der Patientenauswahl und Auswahl der Zielläsionen ungelöst.
Das INTERACT-Register und die geplanten randomisierten Arme der INTERACT-Studie werden entscheidende Informationen über häufige Chancen und Herausforderungen bei der Integration von SBRT in umfassende Behandlungskonzepte bei metastasierter Krebserkrankung liefern. Die begleitenden translationalen Analysen haben das Ziel, das Fortschreiten an bestehenden oder neuen Metastasen bei Patienten mit unterschiedlichen Tumorhistologien und Behandlungshistorien vorherzusagen.
Wichtigste Einschlusskriterien
- ECOG 0/1
- Alter ≥ 18 Jahre
- histopathologisch bestätigte solide Tumorerkrankung mit Metastasen in der Bildgebung
- relevante metastatische Läsionen können basierend auf der Bewertung durch den behandelnden Radioonkologen mit einer ablativen Dosis (≥ 50 Gy BED10) behandelt werden
- die weitere Anwendung systemischer Therapien wurde festgelegt
Wichtigste Ausschlusskriterien
- erhebliche Überlappungen der Metastasenlokalisation mit einer durch Bestrahlung vorbehandelten Region, ein Einhalten der Dosis-Constraints verhindert
- Ausbreitung der Metastasen in den GI-Trakt (Ösophagus, Magen, Dünn- oder Dickdarm), mesenteriale Lymphknoten, oder die Haut
- maligner Pleuraerguss oder maligner Aszites
Alle Patienten die bereit sind eine Randomisierung zu durchlaufen, werden in die entsprechenden Arme der Phase-II-Studie eingeschlossen. Alle anderen Patienten, die die Kriterien erfüllen, werden in das INTERACT-Register eingeschlossen.
MIGNITE
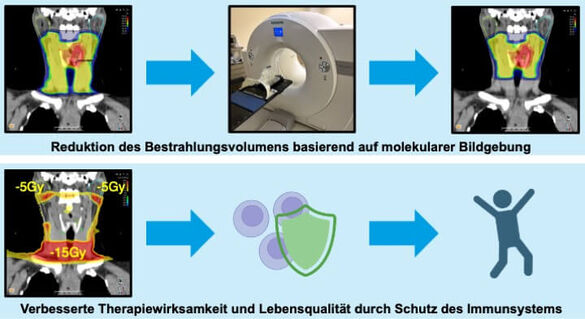
Kann die Anpassung von Zielvolumen und Dosisverschreibung basierend auf molekularer Bildgebung das Immunsystem schützen und die Verträglichkeit der Therapie verbessern?
Zusammenfassung
Die Strahlentherapie ist ein wesentlicher Pfeiler in der definitiven Behandlung von Plattenepithelkarzinomen des Kopfes und Halses (HNSCC). Für diese Behandlungssituation strebt die MIGNITE-Studie an, die akute hochgradige Strahlentoxizität zu verringern, indem die Diagnose und Lokalisierung von Lymphknotenmetastasen durch molekulare Bildgebung in die Strahlentherapieplanung systematisch integriert wird. Der klinische Standard für die Planung der Strahlentherapie bei HNSCC ist bislang die kontrastmittelgestützte Computertomographie (CT). Aufgrund der suboptimalen Sensitivität der CT werden bei der Bestrahlung regelmäßig klinisch unbeteiligte Halslymphknoten mit einbezogen, um inapparente Metastasen zu beseitigen. Im Vergleich zur CT wurde wiederholt gezeigt, dass [18F]Fluordesoxyglucose Positronen-Emissions-Tomographie (FDG-PET) und dessen Kombination mit Magnetresonanztomographie (MRT) zervikale Lymphknoten mit hoher Genauigkeit beurteilen kann. Die MIGNITE-Studie testet zum ersten Mal eine durch molekulare Bildgebung gesteuerte involved-node Strahlentherapie beim HNSCC.
Wichtigste Einschlusskriterien
- neu diagnostiziertes, nicht-metastasiertes Plattenepithelkarzinom in Mundhöhle, Oropharynx, Hypopharynx und Larynx mit geplanter definitiver Radio(chemo)therapie
- molekulare Bildgebung zur Therapieplanung
- Alter ≥ 18 Jahre
- ECOG 0/1
Wichtigste Ausschlusskriterien
- vorangegangene Neck Dissection oder ausgedehnte chirurgische Resektion
- vorangegangene Radiotherapie im Kopf-Hals-Bereich
- T1-2 N0 Larynxkarzinom
NAVIGATORR
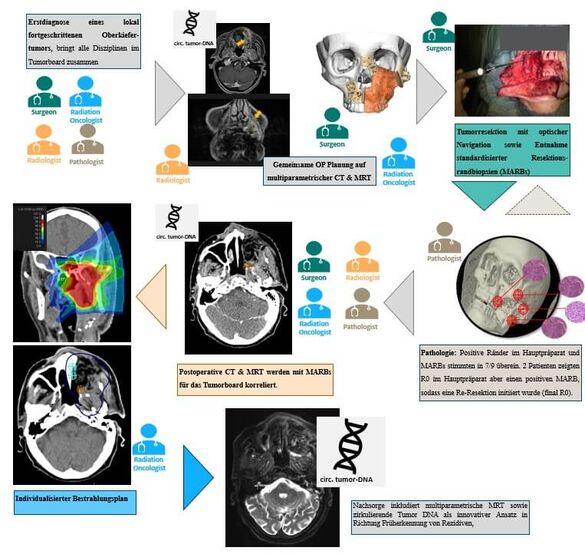
Lässt sich die lokale Kontrolle von Kopf-Hals-Tumoren durch eine enge interdisziplinäre Zusammenarbeit mit einer präziseren chirurgischen Resektion und einer individualisierten adjuvanten Bestrahlung verbessern?
Zusammenfassung
Übergeordnetes Ziel der NAVIGATORR-Studie ist es, die lokale Kontrolle von Kopf-Hals Malignomen durch eine erhöhte Präzision der chirurgischen Resektion in Kombination mit einer individualisierten adjuvanten Bestrahlung zu verbessern. Die primäre Resektion ist in lokal begrenzten Tumoren die Therapie der Wahl. Die Durchführung der Resektion und der Schnittrandkontrolle ist in Grundzügen in den letzten Jahrzehnten unverändert geblieben und der Anteil befallener Resektionsränder stagnierte in den vergangenen Jahren auf einem relativ hohen Niveau.
Im Rahmen der NAVIGATORR Studie sollen Patienten mit Kopf-Hals Malignomen des Mittelgesichts einer navigationsgestützten Tumorresektion unterzogen werden. Dabei soll ein interdisziplinärer Austausch der intraoperativen Navigationsdaten zwischen Chirurgen, Pathologen und Strahlentherapeuten etabliert werden. Primärer Endpunkt ist das Erreichen einer “clear margin” (Tumorabstand vom Resektionsrand > 5 mm). Darüber hinaus sollen beispielsweise die Dosisverteilung der mittels Navigationsdaten geplanten Bestrahlung, die lokale Tumorkontrolle oder das Gesamtüberleben analysiert werden.
Wichtigste Einschlusskriterien
- Tumorerkrankung des Mittelgesichts, Oberkiefer oder der Schädelbasis (Plattenepithelkarzinom, Adenokarzinom, Mukoepidermoidkarzinom oder adenoid-zystisches Karzinom)
- Indikation zur chirurgischen Tumorresektion nach Empfehlung eines multidisziplinären Tumorboards
- wahrscheinliche Indikation für eine postoperative Radiotherapie
- Patientenalter ≥ 18 Jahre
Wichtigste Ausschlusskriterien
- Kontraindikationen gegen Bestrahlung, vor allem schwangere oder stillende Frauen
OLYMPIC
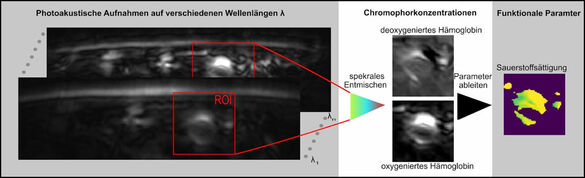
Etablierung der funktionellen, nicht-invasiven Bildgebungsmethode von MSOT als diagnostische Maßnahme zur Hypoxie-Darstellung von cervikalen Lymphknotenmetastasen unter Strahlentherapie
Zusammenfassung
Die multispektrale photoakustische Tomographie (MSOT) bietet eine nicht-invasive, kosteneffiziente und strahlungsfreie Möglichkeit zur Echtzeitabbildung lichtabsorbierender im menschlichen Gewebe. Durch diese Technik kann zum Beispiel die Blutsauerstoffsättigung (sO2) bis in mehrere Zentimeter Tiefe räumlich erfasst werden.
Die Hypoxie (Sauerstoffmangel im Gewebe) ist ein zentrales Element der Strahlenresistenz von Tumoren, weshalb die Bedeutung der Hypoxie in der Radioonkologie zunimmt. Eine molekulare Bildgebung wie MSOT könnte eine Lösung für die Probleme der bisher genutzten Hypoxie-Messmethoden bieten, da sie in der Lage ist, Tumorhypoxie nicht-invasiv, kostengünstig und schnell darzustellen. Unsere MSOT-Pilotstudie (Veröffentlichung ausstehend), zeigte die Durchführbarkeit der Methode in-vivo und vielversprechende Ergebnisse bzgl. der Tumorhypoxiemessung in befallenen Lymphknoten. Allerdings ergaben sich aus dieser explorativen Vorstudie auch viele Herausforderungen.
In dieser Folgestudie soll nun eine deutlich höhere Patientenzahl untersucht werden, u.a. um die Verbesserungen der postprozeduralen Nachbearbeitung zur Anwendung kommen zu lassen, aus den Fehlern der Pilotstudie zu lernen und dabei das klare Studienziel der Darstellung der Tumorhypoxie und seiner Dynamik während der Strahlentherapie zu verfolgen. Ein besonderes Augenmerk soll dabei auf der Korrelation der MSOT-Signale (Sauerstoffsättigung, Blutvolumen) mit Parametern aus der klinischen Routine (MRT, CT, PET-CT, Pathologie, Sonographie) liegen. Unser übergeordnetes Ziel ist dabei, MSOT als funktionelle, nicht-invasive Bildgebungsmethode zur Evaluation der Tumorhypoxie von cervikalen Lymphknotenmetastasen bei Patienten mit Kopf-Hals-Tumoren oder Hauttumoren im Kopf-Hals-Bereich unter Strahlentherapie zu etablieren.
Wichtigste Einschlusskriterien
- Patienten mit zervikalen Lymphknotenmetastasen eines Kopf-Hals- oder Hauttumors im Kopf-Hals-Bereich
- Geplante Strahlentherapie
- Abgeschlossene Wundheilung nach chirurgischer Intervention
- KI ≥ 60%
- Alter ≥ 18 Jahre
- Patientenaufklärung und schriftliche Einwilligung
Wichtigste Ausschlusskriterien
- Ablehnung einer möglichen Rasur im Untersuchungsgebiet
- Patient ist nicht einwilligungsfähig
- Schwangere oder stillende Frauen
PROFOUND-HN
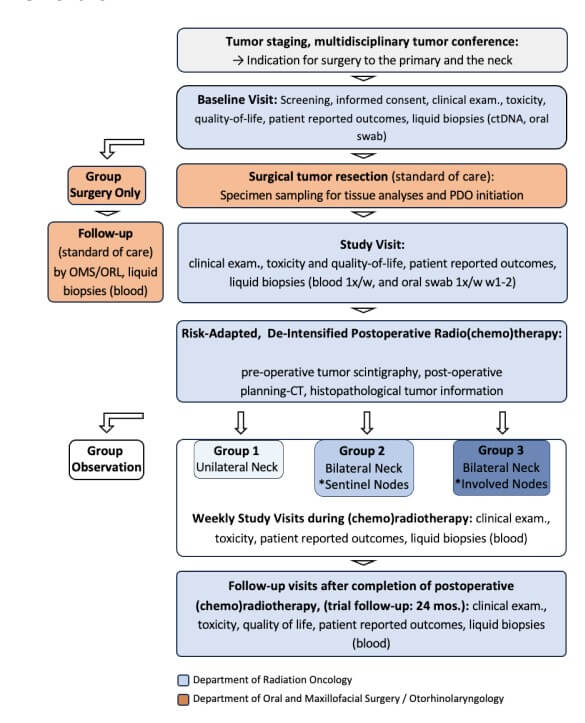
Kann das elektive Zielvolumen in der postoperativen Bestrahlung von Kopf-Hals-Tumoren basierend auf molekularer Bildgebung verkleinert und damit eine bessere Verträglichkeit bei weiterhin guter Tumorkontrolle erreicht werden?
Zusammenfassung
Die postoperative Strahlentherapie ist ein wichtiger Bestandteil der Therapie fortgeschrittener Kopf-Hals-Tumore. Dabei werden standardmäßig die „Hochrisiko-Region“ des präoperativen Tumorbefalls sowie zusätzlich elektive „Niedrigrisiko-Regionen“ bestrahlt. Der elektiven Bestrahlung des zervikalen Lymphabflusses zur Eradikation mikroskopischer, unerkannter Tumorzellaussaat steht eine höhere Dosisbelastung von für Lebensqualität und Schluckfunktion wichtiger Strukturen gegenüber.
Die PROFOUND-HN-Studie nutzt die Integration von präoperativer molekularer Bildgebung, sowohl zur Steuerung der Halsdissektion im Rahmen der Tumoroperation, als auch zur risikoadaptierten Planung der postoperativen Strahlentherapie. Die Bestrahlung elektiver Halsregionen wird auf 2 cm kranio-kaudal der bildmorphologisch und/oder pathologisch bestätigten befallenen Lymphknoten begrenzt, was eine systematische Volumenreduktion der bestrahlten Niedrigrisiko-Regionen bewirkt. Eine gänzlich einseitige Halsbestrahlung wird für Patient*innen mit geeignetem Risikoprofil, wenn immer möglich, durchgeführt, um Mittellinienstrukturen des Schluckapparates bestmöglich zu schonen.
Ziel ist es, dadurch die Toxizität bei guter Tumorkontrolle zu senken und damit die Lebensqualität der Patienten zu steigern.
Wichtigste Einschlusskriterien
- neu diagnostiziertes, nicht metastasiertes Plattenepithelkarzinom der Mundhöhle, des Oropharynx, Hypopharynx oder Larynx
- Indikation zur chirurgischen Tumorresektion
- mögliche Indikation zur postoperativen Radio(chemo)therapie
Wichtigste Ausschlusskriterien
- frühere Bestrahlung im Kopf-Hals-Bereich
- große Operationen der Mundhöhle, des Pharynx, Larynx oder der Halsregion
- bekannte metastasierte Erkrankung
Ausgewählte Publikationen
Janke, F., Stritzke, F., Dvornikovich, K., Franke, H., Angeles, A. K., Riediger, A. L., Ogrodnik, S., Gerhardt, S., Regnery, S., Schröter, P., Bauer, L., Weusthof, K., Görtz, M., Harrabi, S., Herfarth, K., Neelsen, C., Paech, D., Schlemmer, H. P., Abdollahi, A., Adeberg, S., Debus J., Sültmann H., Held, Th. (2024). Early circulating tumor DNA changes predict outcomes in head and neck cancer patients under re-radiotherapy. International journal of cancer, 10.1002/ijc.35152. Advance online publication. doi.org/10.1002/ijc.35152
Weusthof, K., Held, Th., Lang, K., Rachel, Z. E., Harrabi, S. B., Plath, K., Freudlsperger, C., Herfarth, K., Debus, J., Haberer, T., Münter, M., Jensen, A. D., & Adeberg, S. (2024). Combined Photon and Carbon Ion Radiation Therapy for Sinonasal Malignancies: Results of the HIT-SNT Prospective Phase 2 Trial. International journal of radiation oncology, biology, physics, 118(5), 1563–1574. doi.org/10.1016/j.ijrobp.2023.09.037
Held, Th., Franke, H., Lang, K., Eichkorn, T., Regnery, S., Weusthof, K., Bauer, L., Plath, K., Dyckhoff, G., Plinkert, P. K., Harrabi, S. B., Herfarth, K., Debus, J., & Adeberg, S. (2022). Intensity modulated proton therapy for early-stage glottic cancer: high-precision approach to laryngeal function preservation with exceptional treatment tolerability. Radiation oncology (London, England), 17(1), 199. doi.org/10.1186/s13014-022-02144-w
Held, Th., Windisch, P., Akbaba, S., Lang, K., El Shafie, R., Bernhardt, D., Plinkert, P., Kargus, S., Rieken, S., Herfarth, K., Debus, J., & Adeberg, S. (2019). Carbon Ion Reirradiation for Recurrent Head and Neck Cancer: A Single-Institutional Experience. International journal of radiation oncology, biology, physics, 105(4), 803–811. doi.org/10.1016/j.ijrobp.2019.07.021